Structure générale des acides alpha aminés
Les acides aminés naturels sont essentiellement des acides a-aminés ayant comme structure générale, une chaîne principale commune (NH2-CH-COOH) et une chaine latérale spécifique pour chacun d'eux (-R).
Un acide a-aminé a donc comme structure générale:
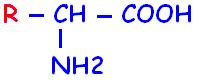
La chaîne latérale permet de classer les acides aminés en fonction de ses propriétés. On distingue 4 groupes :
acide, basique, hydrophile (polaire) et hydrophobe (apolaire).
Propriétés ioniques des AA
En solution, les groupement carboxyle -COOH acide et amino -NH2 basique existent sous deux formes : chargée et neutre.
R-COOH <--> R-COO- + H+ et R-NH3+ <--> R-NH2 + H+
Les AA sont des structures diioniques amphotères. Dans une solution, en fonction du pH, les AA existent sous 3 formes:

En milieu acide, le groupement amine s'ionise en captant un proton. Le pK de COO- ou pKa (pH de dissociation) est d'environ 2/3.
En milieu basique, le groupement acide s'ionise en libérant un proton. Le pK NH3+ ou pKb (pH de dissociation) est d'environ 9/10.
Au niveau du point isoélectrique (pHi) les 2 groupements sont ionisés. Le pHi = (pKa +pKb)/2
La chaine radicale peut aussi être ionisable (exemple: la tyrosine), et le groupement a lui aussi un pK appelé pKr. Dans ce cas le pHi se calcule en fonction des 2 groupements de même polarité.
Pour l'acide aspartique (AA diacide) : pKa = 2,2 / pKb = 9,8 / pKr = 3,9 / pHi = 3,0 avec pHi = (pKa + pKr)/ 2
Pour la lysine (AA dibasique) : pKa = 2,2 / pKb = 9,0 / pKr = 10,5 / pHi = 9,8 avec pHi = (pKb + pKr) / 2
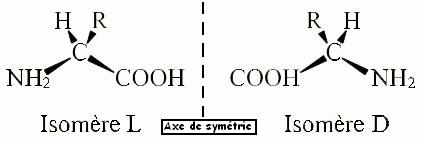
Les AA et l'isomérie
Le carbone central de la chaîne principale est appelé par convention carbone alpha. Il porte, en plus de son hydrogène, trois groupements chimique.
Si c'est 4 groupements sont différents le carbone alpha est axymétrique et la molécule est dite chirale.
Pour les acides a-aminés, à l'exception de la glycine, tous sont chiraux (comme vos 2 mains, elles ne peuvent pas se superposer).
C'est AA chiraux existent sous 2 formes appelés isomères ou stéréoisomères : L et D.
En effet selon la forme de l'AA (molécule optiquement active) la lumière plane polarisée est déviée soit dans le sens des aiguilles d'une montre et
on parle d'isomère dextrogyre,
soit dans le sens inverse des aiguilles d'une montre (ou sens anti trigonométrique) et on parle d'isomère lévrogyre.
Pour les AA comportant 2 carbones assymétriques (exple: thréonine) on parle d'allo-isomères.
La forme L des AA est la plus présente dans les protéines. Les AA D sont surtout présents dans les parois cellulaires bactériennes.
Les 20 acides alpha-aminés naturels composant les protéines
Les AA aliphatiques hydrophobes
|
Glycine (Gly ou G)
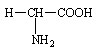
(Acide aminoacétique) |
Alanine (Ala ou A)

Acide L-2-aminopropionique |
Valine (Val ou V)
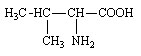
Acide 2-amino-3-méthylbutyrique |
Leucine (Leu ou L)
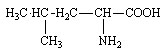
Acide 2-amino-4-méthylvalérique |
Isoleucine (Ile ou I)
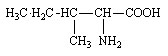
Acide 2-amino-3-méthylvalérique |
Proline (Pro ou P)
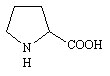
Acide 2-pyrrolidine-carboxylique (Acide iminé) |
Les AA aromatiques hydrophobes
Phénylalanine (Phe ou F)

Acide (S) - alpha - amino - bêta - phenylpropionique |
Tryptophane (Trp ou W)
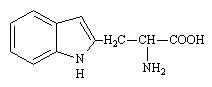
Acide (S) - alpha - amino - bêta - (3 - indolyl) - propionique |
Les AA amidés
Asparagine (Asn ou N)
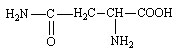
Acide 2-aminosuccinamique |
Glutamine (Gln ou Q)

Acide L-2-aminoglutaramique |
Les AA aromatiques hydroxylés
Tyrosine (Tyr ou Y)
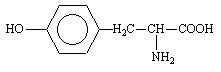
Acide (S) - 3 - (p - Hydroxyphényl) alanine ou Acide (S) - 2 - Amino - 3 - (p - hydroxyphényl) propionique |
Les AA hydrophiles hydroxylés
Sérine (Ser ou S)
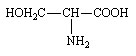
(Acide L-2-amino-3-hydroxypropionique) ou (L-3-Hydroxy-alanine) |
Thréonine (Thr ou T)
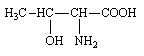
(Acide 2-amino-3-hydroxybutyrique) |
Les AA thiolés (ou soufrés)
Méthionine (Met ou M)

Acide L-2-amino-4-méthylthiobutyrique |
Cystéine (Cys ou C)
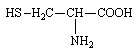
Acide L-2-amino-3-mercaptopropionique |
Les AA diacides (chargés négativement)
Acide aspartique (Asp ou D)
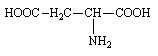
Acide 2-aminosuccinique |
Acide glutamique (Glu ou E)

Acide L-glutaminique |
Les AA dibasiques (chargés positivement)
Lysine (Lys ou K)
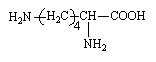
Acide 2,6 - diaminohexanoique |
Arginine (Arg ou R)

Acide (S) - 2 - amino - 5 - guanidinovalérique |
Histidine (His ou H)
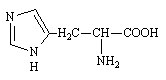
Acide (S) - alpha - amino - 1H - imidazole - 4 - propionique |